本报告基于2017年度国家药品监管部门对血液制品的批签发数据,进行了系统性分析,旨在揭示该年度血液制品的市场供应、产品质量监控状况及行业发展趋势。血液制品作为关乎公共卫生安全和国家战略储备的特殊药品,其批签发数据是衡量行业运行与监管效能的关键指标。
一、 总体批签发情况概览
2017年,我国血液制品批签发总量继续保持稳步增长态势。全年累计批签发批次较2016年有显著提升,反映出国内采浆量供应能力的改善以及生产企业产能的逐步释放。从产品大类看,人血白蛋白、静注人免疫球蛋白(pH4)、人凝血因子VIII等主要品种的批签发量均占据主导地位。其中,人血白蛋白的批签发量依旧最大,满足了临床基础性需求;凝血因子类制品批签发量的增长,则体现了对血友病等罕见病治疗需求的进一步覆盖。
二、 主要品种结构分析
- 人血白蛋白:作为市场份额最大的品种,2017年国产与进口人血白蛋白的批签发比例呈现动态平衡。国产占比稳步提高,但进口产品仍占据重要份额,保障了市场供应的充足与稳定。
- 免疫球蛋白类:静注人免疫球蛋白(pH4)的批签发量稳中有升,其在感染性疾病、自身免疫病等领域的临床应用需求持续。特异性免疫球蛋白(如破伤风、乙肝等)的批签发相对稳定,服务于特定预防与治疗场景。
- 凝血因子类:人凝血因子VIII的批签发量增长明显,得益于企业技术进步与产能扩张,对缓解国内血友病患者用药紧张局面起到了积极作用。其他凝血因子制品批签发规模相对较小,但需求刚性。
- 其他制品:包括人纤维蛋白原等,批签发量较小,但在外科止血等特定医疗环节中不可或缺。
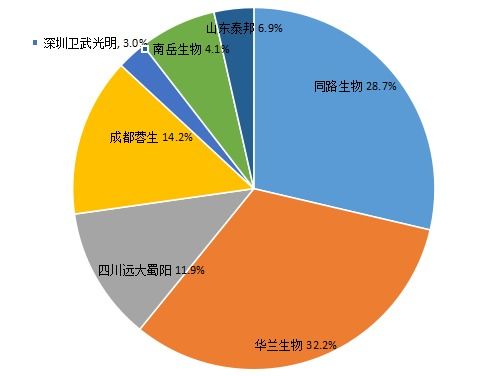
三、 生产企业格局分析
2017年的批签发数据显示,血液制品行业集中度较高,主要批签发量集中于少数几家大型生物制品企业。这些企业凭借其浆站资源、生产规模与技术优势,构成了市场供应的主力军。数据也反映出部分企业正在通过技术改造和新产品开发,积极拓展其产品线与市场份额,行业内部竞争态势持续。
四、 质量监控与批签发合格率
2017年度血液制品批签发检验的总体合格率维持在高位水平,这体现了国家药品监管部门对血液制品从原料血浆到成品出厂的全链条严格监管取得了实效,也反映了主流生产企业质量体系的稳健运行。不合格批次(如有)的主要因素集中于个别项目的检定不符合规定,监管部门均依法进行了处理,有效拦截了潜在风险产品流入市场,保障了用药安全。
五、 趋势与展望
通过对2017年数据的分析,可以看出:1) 国内血液制品供应能力持续增强,但结构性矛盾(如凝血因子等特定品种的相对短缺)仍需通过产业升级逐步解决;2) 行业监管体系日趋严格与完善,批签发制度作为上市前最后一道质量关口,其权威性和有效性持续巩固;3) 随着医疗需求增长和医保政策覆盖深化,血液制品市场预计将保持稳定增长,对产品的安全性、有效性和可及性提出了更高要求。
2017年的血液制品批签发数据,清晰地勾勒出行业在保障供应、提升质量与加强监管方面取得的进展。在“健康中国”战略引领下,血液制品行业需进一步优化产业结构,加强科技创新与质量管理,以更安全、充足、多样的产品满足人民群众日益增长的健康需求,并为国家公共卫生安全提供坚实保障。