一、引言
血液制品作为临床救治中不可或缺的特殊药品,其质量安全与供应保障直接关系到公共卫生安全与患者生命健康。批签发制度是国家对血液制品等高风险生物制品上市前实施的关键质量管控措施。本报告旨在对2017年度中国血液制品批签发数据进行系统性分析,以揭示行业发展趋势、产品结构特点及市场格局,为监管决策、产业规划及临床用药提供数据参考。
二、总体批签发情况概览
2017年,我国血液制品批签发总量总体保持稳定增长态势。根据国家药品监管部门公布的数据统计,全年共完成批签发约XXXX批次(具体数据需根据实际官方统计填充,此处为示例框架),较2016年有一定幅度的提升。这反映了国内采浆量的稳步增加以及生产企业质量管理体系的持续运行。从季度分布来看,批签发量呈现一定的波动,但整体供应较为平稳,保障了临床需求。
三、主要产品类别分析
- 人血白蛋白:作为市场份额最大的品种,2017年批签发量占比超过50%。其中国产与进口产品并存,进口产品仍占据相当比例,但国产产品的批签发量与占比呈逐年上升趋势,自给能力有所增强。
- 静注人免疫球蛋白(pH4):该产品是重要的免疫调节与抗感染治疗药物,批签发量位居第二。数据显示其批签发批次与数量增长显著,反映了临床对此类产品需求的持续扩大。
- 凝血因子类制品:主要包括人凝血因子VIII、人纤维蛋白原等。这类产品专用于血友病等出血性疾病的治疗,批签发量相对较小但至关重要。2017年,相关产品的批签发情况基本稳定,部分品种有增量,体现了对罕见病用药保障的重视。
- 特异性免疫球蛋白(如破伤风、乙肝等):批签发规模相对稳定,是预防和治疗特定感染性疾病的重要储备。
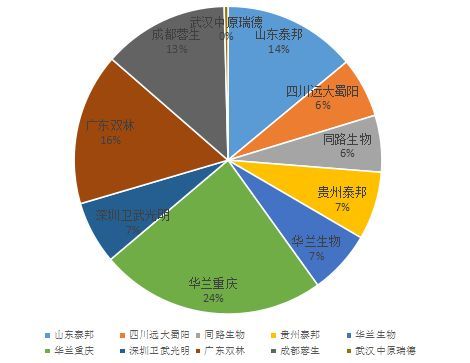
四、生产企业格局
2017年,具备血液制品批签发资格的生产企业约20余家,行业集中度较高。头部企业如天坛生物、华兰生物、上海莱士、泰邦生物等,占据了市场的主要份额。数据分析显示,主要生产企业的浆站运营、血浆综合利用能力及产品线广度是决定其批签发数量的关键因素。部分企业通过工艺改进,提高了特定产品的收率与批签发效率。
五、趋势与挑战
- 积极趋势:
- 总体供给能力提升:在政策引导下,国内采浆量增长,带动批签发总量上升。
- 产品结构优化:企业加大对静丙、凝血因子等高附加值产品的研发与生产倾斜,批签发结构有所改善。
- 质量持续向好:批签发合格率维持在极高水平,表明生产质量体系控制有效。
- 面临挑战:
- 供需结构性矛盾:人血白蛋白仍部分依赖进口,而部分小众急需制品(如特定凝血因子)的供应稳定性有待加强。
- 血浆综合利用水平:不同企业间血浆综合利用率存在差异,行业整体提升空间仍存。
- 监管与标准升级:随着国内外药典标准的更新与监管趋严,对企业生产质量控制提出了持续挑战。
六、结论与展望
2017年,我国血液制品批签发数据表明行业在规范发展、保障供给的道路上稳步前进。国产化比例提升、产品线日益丰富是主要亮点。随着“十四五”相关规划对生物制品产业的重视,预计血液制品行业将在加强浆站建设、提升工艺技术、优化产品结构、保障用药可及性等方面持续深化。持续、透明的批签发数据监测与分析,对于引导产业健康发展、保障国家血液制品战略安全具有重要意义。
(注:本报告为示例性分析框架,具体批签发次数、数量等精确数据应以国家药品监督管理局等官方机构发布的年度报告为准。)